Programas de garantía externa de la calidad SEQCML. Evolución de las prestaciones analíticas de los laboratorios clínicos a lo largo de 30 años y comparación con otros programas
-
Carmen Perich Alsina
, Carmen Ricós
Abstract
Objetivos
El objetivo de este estudio es conocer la evolución de la prestación analítica de los laboratorios participantes en los programas EQA de la SEQCML durante los 30 años de funcionamiento y compararla con la prestación obtenida en otros programas EQA para saber si los resultados son similares.
Métodos
Se evalúan los resultados obtenidos durante este periodo, aplicando las especificaciones de la calidad derivadas de la VB y del estado del arte. Además, se realiza una comparación con los resultados obtenidos por otras organizaciones de programas EQA.
Resultados
Se observa que los laboratorios participantes en los programas EQA-SEQCML han mejorado su prestación durante los 30 años de experiencia y que las especificaciones derivadas de la variación biológica son alcanzables. La comparación entre programas EQA es difícil, debido a: la falta de accesibilidad y a las diferencias en el diseño de estos programas (materiales control, cálculos empleados y especificaciones analíticas establecidas).
Conclusiones
Los datos de este estudio ponen de manifiesto que para algunas magnitudes biológicas los resultados obtenidos en los programas todavía no están armonizados, aunque se estan realizando esfuerzos para alcanzar la armonización. Los organizadores de programas EQA deberían sumarse al esfuerzo de armonización, facilitando la información sobre sus resultados para permitir su comparación.
Introducción
Los programas de garantía externa de la calidad (EQA) son un componente fundamental de la gestión de la calidad de los laboratorios. Su participación permite al laboratorio evaluar y monitorizar su prestación analítica, comparar la fiabilidad de los procedimientos de medida y conocer el grado de armonización de los resultados analíticos.
La Sociedad Española de Medicina de Laboratorio (SEQCML) puso en marcha su primer programa EQA en1981, incluyendo 20 magnitudes bioquímicas en suero y con 147 participantes [1]. Desde entonces, se han incorporado programas propios y se han establecido colaboraciones con programas nacionales y europeos (Sociedad Española de Hematología y Hemoterapia para magnitudes hematológicas, UK NEQAS para las de inmunología y alergia, y OELM para elementos traza). En la actualidad, la SEQCML distribuye 29 programas que abarcan todas las áreas del laboratorio, cubriendo 189 magnitudes biológicas y en los que participan alrededor de 700 laboratorios.
La información que ha de facilitar un programa EQA según el Task Group on performance specifications for EQAS de la European Federation of Clinical Chemistry and Laboratory Medicine (EFLM-TG-EQA) creado en la 1a Conferencia estratégica de Milán en 2014 [2], para que los participantes puedan interpretar correctamente sus resultados [3] concierne a: el material control distribuido, el valor diana al que se compara el resultado del laboratorio, cómo se expresa la prestación analítica del participante y el criterio de evaluación utilizado.
El material control de la mayoría de los programas EQA de la SEQCML es suero estabilizado excepto el programa de suero conmutable con valores asignados por método de referencia (SCR) que utiliza suero humano congelado.
El valor diana de las muestras control es el valor medio obtenido por cada grupo de usuarios del mismo método analítico e instrumento (grupo homogéneo o grupo par), y el del programa SCR es el valor de referencia certificado.
La prestación analítica del laboratorio se expresa mediante la desviación porcentual (DP%) de cada resultado respecto al valor diana, indicativo del error total (ET) analítico. La prestación analítica de los métodos participantes se expresa mediante el coeficiente de variación (CV) inter-laboratorios , que indica la imprecisión de cada grupo homogéneo y mediante la DP% de la media de cada grupo homogéneo que indica el sesgo del método.
El criterio de evaluación ha variado con los años: hasta 1993 se usaba el criterio estadístico de la puntuación estándar respecto al grupo homogéneo [4]. A partir de 1994 se aplicó, además, la especificación de calidad analítica (EPA) derivada de la variabilidad biológica (VB) cuando existían datos disponibles [5] y en caso contrario, a partir del 2011, el percentil 90 de los resultados de las desviaciones individuales (DP%) obtenidas por los participantes, una vez excluidos los valores extremos.
En el caso de utilizar VB, se emplean tres “niveles” de exigencia, denominados mínimo, deseable y óptimo [6], según el porcentaje de desviaciones individuales de los laboratorios que cumplen la especificación:
Mínimo: menos del 80% de las DP lo cumplirían
Deseable : entre un 80 y un 90%
Óptimo: un 90% o más DP estarían dentro del límite definido por la VB.
Siguiendo la tipificación de los programas EQA descrita por Miller y cols [7] la mayor parte de los programas de la SEQCML son de categoría 4 (material control de suero humano estabilizado, valor asignado por el grupo homogéneo, medidas repetidas, EPA basadas en la VB); el programa SCR es de categoría 1 (material control de suero humano congelado, valor asignado por método de referencia, medidas repetidas, EPA basadas en la VB).
Los objetivos de este estudio son:
conocer la evolución de la prestación analítica de los laboratorios participantes en los programas EQA de la SEQCML a lo largo de más de 30 años de funcionamiento (1981 – 2018), y
comparar la prestación analítica obtenida por los laboratorios participantes en los programas EQA de la SEQCML con la de los participantes en otros programas EQA.
Materiales y métodos
El material empleado en este estudio son los informes para el laboratorio individual y de final de ciclo, que los programas EQA de la SEQCML proporcionan a los participantes.
Informe para el laboratorio individual
Ha evolucionado con el tiempo, cumpliendo actualmente las recomendaciones del EFLM-TF-EQA [3]. Los datos incluidos son:
histograma de distribución de resultados
número de resultados recibidos
número de resultados incluidos en los cálculos estadísticos (se excluyen los valores aberrantes, que exceden el intervalo media ± 3 desviaciones estándar reiterativamente hasta que no queda ningún dato fuera de dicho intervalo) [8]
media y desviación estándar de todos los participantes, del mismo método que el participante y del mismo método e instrumento (grupo homogéneo),
resultado obtenido por el laboratorio y su desviación respecto al valor diana, expresada en puntuación estándar y en porcentaje
desviación porcentual aceptable según el criterio derivado de la VB para el ET analítico, habiéndose añadido en el año 2005 una gráfica con los resultados de los últimos 12 meses y su desviación respecto a la VB (Supplementary Figura 1).
En el programa SCR el informe incluye:
desviación porcentual respecto al valor de referencia de las six muestras,
coeficiente de variación (obtenido entre los replicados control) del laboratorio,
media, coeficiente de variación y desviación porcentual de la media del grupo homogéneo (mismo método, instrumento y trazabilidad) respecto al valor de referencia (Supplementary Figura 2).
Siguiendo su objetivo educativo, la organización elabora y envía notas técnicas relacionadas con los programas para ayudar a los participantes en la interpretación de los resultados. Asimismo, mantiene una comunicación bidireccional para cualquier consulta que los laboratorios participantes deseen realizar.
Informe de fin de ciclo
Contiene los indicadores de la prestación analítica de los métodos participantes:
Coeficiente de variación inter-laboratorios de los grupos homogéneos.
Sesgo de los grupos homogéneos (diferencia entre la media del grupo y el valor diana).
Percentiles de la desviación de cada resultado respecto al grupo homogéneo (DP%), desde el año 2011. Inicialmente se mostró el percentil 90 (P90) pero, a partir del año 2017, se muestran también P20, P50 y P70 para que cada laboratorio pueda seleccionar su especificación.
El método utilizado es la inspección visual de los informes de fin de ciclo emitidos desde 1981 hasta 2018, la cuantificación del porcentaje de resultados que cumplen las EPA y la comparación visual de los indicadores con respecto a los de programas de otros países.
Resultados
Evolución de la prestación analítica de los laboratorios participantes en los programas EQA de la SEQCML
A partir del informe individual se obtiene la desviación respecto al grupo par. En la Figura 1 se muestra el porcentaje de resultados individuales de los laboratorios (obtenida del informe individual) en el año 2018, cuya desviación (DP%) respecto al grupo homogéneo cumple con la especificación de calidad para ET analítico derivada de la VB (mínima, deseable u óptima), en el programa de bioquímica en suero.
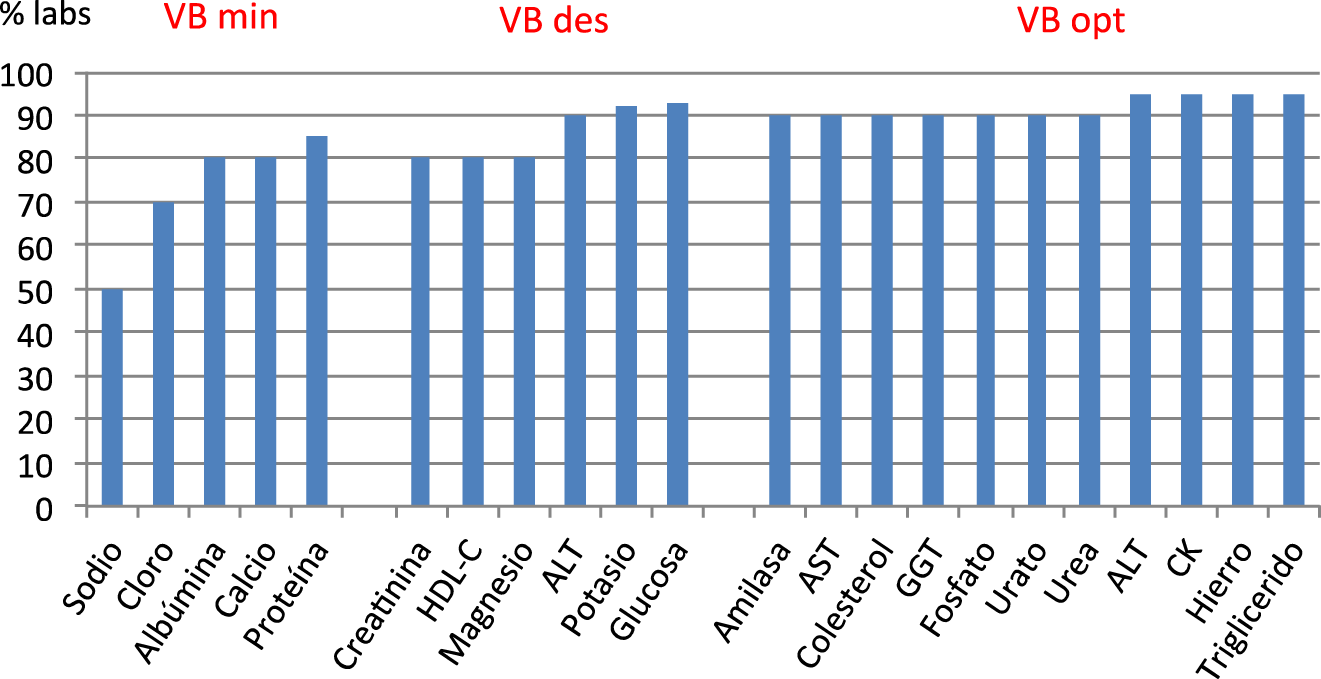
Cumplimiento de la especificación para error total analítico derivada de la VB en el programa de Bioquímica suero del 2018.
Para la mayoría de las magnitudes biológicas, el 90% de los resultados de los participantes cumplen con la especificación e incluso para las magnitudes con una mayor regulación homeostática (menor VB y especificaciones más restrictivas), el 50% o más de los laboratorios es ya capaz de cumplir el requisito.
Si se compara la DP% del percentil 90 de los laboratorios participantes en el programa de hormonas entre los años 2012 y 2018, se observa una disminución muy importante (Supplementary Figura 3). El 90% de los resultados de insulina de los laboratorios en el año 2012 obtenía DP = 39% que ha disminuido a DP = 14% en el 2018. Asimismo, el P90 de los resultados de péptido C ha disminuido de 23% a 14% y los de tirotropina del 13% al 9%.
A partir del informe de fin de ciclo se obtienen los indicadores de imprecisión inter-laboratorios (medida como CV) y sesgo respecto al grupo homogéneo (medido como DP%). En la Figura 2 se muestran cinco cortes temporales de magnitudes escogidas como representativas de sustratos (glucosa), electrolitos (potasio), enzimas (ALT) y hormonas (TSH)
Glucosa (Figura 2A): el uso mayoritario de los métodos enzimáticos a partir de los años 90 disminuyó la imprecisión inter-laboratorios al 6% y el sesgo al 10%. Con el uso de métodos enzimáticos mas específicos, en el año 2018 se obtuvo un CV del 4% y una DP del 7%.
Potasio (Figura 2B): en el año 1984 existían más de diez métodos diferentes para analizar potasio, con un CV del 5,5% y un sesgo del 7%; desde 1989 hasta el año 2000 coexistieron la fotometría de llama y la potenciometría y posteriormente solo la potenciometría. Los indicadores de prestación analítica han mejorado paulatinamente hasta obtener un CV del 2% y un sesgo del 2% en el año 2018.
ALT (Figura 2C): al igual que en otros enzimas, la desaparición de métodos colorimétricos produjo una reducción de la imprecisión inter-laboratorios, desde CV cercanos al 50% hasta CV inferiores al 5%. También el sesgo disminuyó espectacularmente.
TSH (Figura 2D): en 1999 se inició el programa de hormonas, utilizándose entonces diferentes métodos analíticos con un CV del 12% y un sesgo del 30%. A partir del 2010, con el uso mayoritario de métodos luminiscentes, el CV ha disminuido al 5% y el sesgo al 15%.
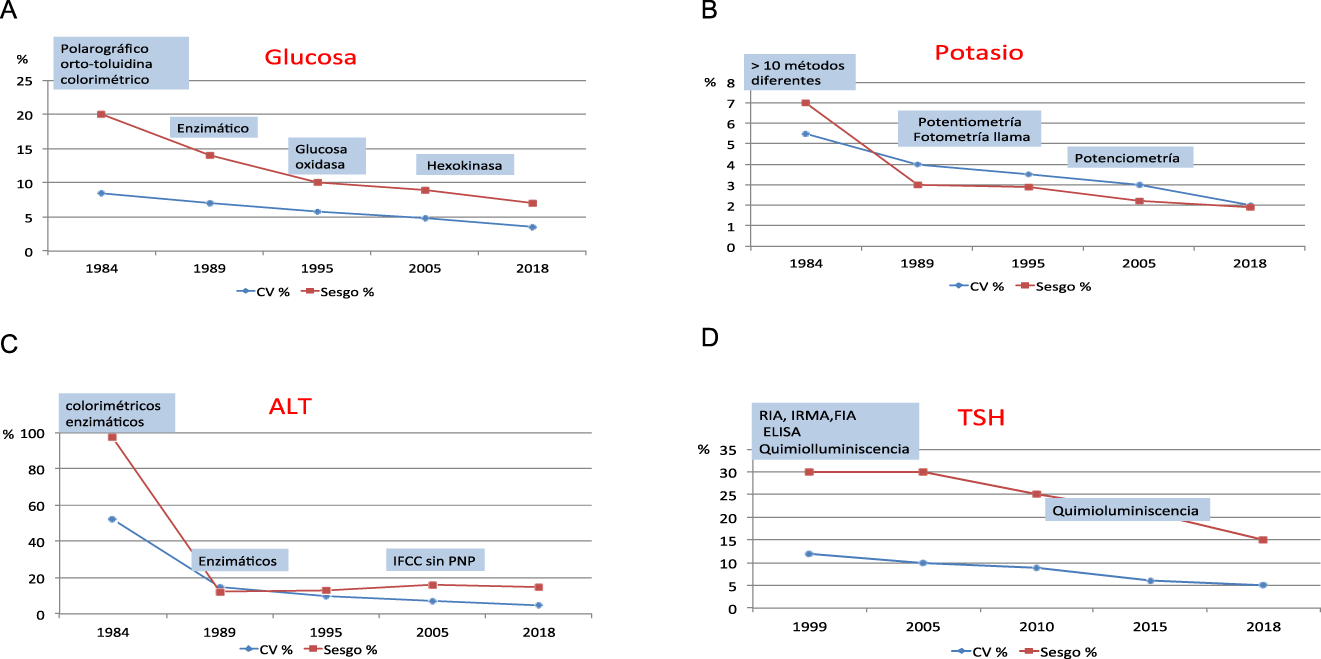
Evolución de la imprecisión inter-laboratorios y del sesgo respecto al grupo homogéneo.
Comparación de los programas EQA de la SEQCML con otros programas EQA
En la Tabla 1 se muestra la imprecisión inter-laboratorios obtenida en el año 2018 por los programas SEQCML (control no conmutable) [8], el programa holandés Stichting Kwaliteitsbewaking Medische Laboratoriumdiagnostiek (SKML) (control conmutable) [9], el belga Empower project (control conmutable) [10] y el alemán Referenzinstitutfür Bioanalytik (control no conmutable) [11], para algunas magnitudes biológicas de bioquímica en suero. En general los CV son similares entre los distintos programas, excepto para ALT (CV entre 4% y 10%) y LDH (CV entre 2.6 y 9.0%).
Imprecisión inter-laboratorios (CV%) obtenida por varios programas europeos en el año 2018.
| Magnitud | SEQC (NC) [8] | SKML (C) [9] | Empower project (C) [10] | RfB (NC) [11] |
|---|---|---|---|---|
| Albúmina | 4,5 | 4,0 | – | 4,7 |
| ALT | 4,9 | 10,0 | 9,1 | 5,5 |
| AST | 5,0 | 7,5 | 3,3 | 5,7 |
| Calcio | 2,3 | 2,0 | – | 2,7 |
| Creatinina | 5,7 | 5,5 | – | 4,4 |
| Fosfato | 3,3 | 4,0 | – | 3,6 |
| GGT | 5,7 | 8,5 | 6,9 | 4,8 |
| Glucosa | 3,4 | 4,0 | – | 3,4 |
| LDH | 5,1 | 9,0 | 2,6 | 4,4 |
| Magnesio | 3,4 | 6,0 | – | 4,0 |
| Potasio | 2,0 | 1,0 | 1,2 | 2,3 |
| Sodio | 1,6 | 0,9 | 0,8 | 1,9 |
| Urato | 2,6 | 3,0 | – | 4,0 |
| Urea | 3,5 | 4,0 | – | 4,8 |
C, muestras conmutables; NC, muestras no conmutables.
En la Tabla 2 se compara visualmente la DP% respecto al grupo par obtenido en los programas SEQCML y en el ProBioQual (Francia) [12]; ambos utilizan material no conmutable y como valor diana el grupo par. Para este indicador se observan mejores resultados en el programa de la SEQCML (DP% visualmente inferiores).
Error total analítico (DP% respecto al grupo par) obtenido por el percentil 90 de los participantes en dos programas europeos.
| Magnitud | SEQCML [8] 2018 | PBQ [12] 2015 |
|---|---|---|
| Fosfatasa alcalina | 10,4 | 15,1 |
| ALT | 7,5 | 11,7 |
| Amilasa | 7,2 | 9,1 |
| AST | 7,8 | 10,8 |
| Bilirrubina | 8,4 | 12,0 |
| Calcio | 4,3 | 5,7 |
| Colesterol | 5,5 | 6,6 |
| Creatina quinasa | 8,3 | 11,8 |
| Cloro | 3,9 | 5,6 |
| Creatinina | 9,2 | 11,0 |
| GGT | 9,7 | 14,1 |
| Glucosa | 5,0 | 7,3 |
| Potasio | 3,2 | 4,6 |
| LDH | 9,9 | 15,2 |
| Lipasa | 11,0 | 13,3 |
| Magnesio | 6,0 | 10,1 |
| Sodio | 2,7 | 3,6 |
| Fosfato | 5,9 | 8,2 |
| Triglicérido | 6,5 | 8,6 |
| Urato | 5,4 | 5,9 |
| Urea | 6,4 | 12,5 |
Controles no conmutables.
Valor diana: media del grupo homogéneo.
En la Tabla 3 se presentan los resultados del año 2018 del sesgo (DP%) obtenido en tres programas que usan controles conmutables con valores asignados por métodos de referencia certificados (SEQCML-SCR, SKML y Empower project) [8, 10, 13]. Los valores que se muestran corresponden a la desviación porcentual entre la media del grupo par más frecuente y el valor de referencia. Los datos corresponden a enzimas determinados por métodos recomendados por IFCC. Se observa un menor sesgo (DP% visualmente inferior) en los resultados de los programas SEQCML y SKML.
Sesgo (DP%) respecto al método de referencia obtenido para enzimas determinados por los métodos recomendados por IFCC (2018).
| Magnitud | SEQC [8] | SKML [10] | Empower project [13] |
|---|---|---|---|
| Fosfatasa alcalina | −6,0 | −10,0 | −15,0 |
| ALT | −16,0 | −14,0 | −25,0 |
| AST | −12,0 | −11,0 | −26,0 |
| Creatina quinasa | 3,0 | 4,0 | – |
| GGT | −5,5 | −8,0 | −15,0 |
| LDH | −8,0 | −5,0 | −18,0 |
En la Tabla 4 se muestran las observaciones publicadas en diferentes estudios [8, 13–16] respecto a la comparabilidad de resultados entre sistemas método-instrumento, utilizando materiales control conmutables. Los autores consideran que existe una buena armonización para urea, colesterol, glucosa, urato y potasio y una pobre estandarización para creatinina, calcio, magnesio, cloro y sodio; mientras que los resultados en proteína y fosfato son discrepantes. Sin embargo, es importante recalcar que estas organizaciones utilizaron distintas EPA (estado del arte, VB), para considerar el grado de armonización de estas magnitudes biológicas.
Grado de comparabilidad entre sistemas método-instrumento según varios estudios.
| Magnitud | SCR SEQC [8] | SKML [13] | Empower [14] | Miller [15] | Van Houcke [16] |
|---|---|---|---|---|---|
| Urea | – | SI | – | SI | – |
| Colesterol | -- | SI | SI | SI | – |
| Glucosa | DEP | SI | SI | SI | – |
| Creatinina | NO | NO | DEP | – | – |
| Fosfato | – | – | SI | DEP | – |
| Proteína | DEP | DEP | SI | – | SI |
| Urato | SI | SI | SI | SI | – |
| Calcio | DEP | NO | NO | – | DEP |
| Magnesio | DEP | DEP | DEP | DEP | DEP |
| Cloro | DEP | NO | DEP | NO | – |
| Potasio | SI | SI | SI | SI | – |
| Sodio | NO | NO | SI | NO | – |
SI, sistemas método-instrumento estandarizados; NO, sistemas método-instrumento no estandarizados; DEP, algunos sistemas están estandarizados y otros no.
Discusión
El material control de un EQA ha de ser similar a las muestras de los pacientes y el valor diana debería determinarse por métodos de referencia certificados [3]. Solo uno de los 29 programas de la SEQC cumple actualmente estas características (SCR), siendo las principales dificultades la no existencia de materiales control conmutables ni de métodos de referencia para todas las magnitudes biológicas del laboratorio clínico.
Si el programa EQA utiliza material conmutable con valor asignado por métodos de referencia, puede evaluar la verdadera exactitud del laboratorio individual, evaluar métodos analíticos, así como estimar el sesgo y promover la estandarización. En caso contrario, solo puede evaluar al laboratorio individual y comparar grupos homogéneos.
Los indicadores de la prestación analítica: ET analítico, imprecisión y sesgo calculados, asi como el tipo de las EPA utilizadas en los programas de la SEQCML para evaluar a los participantes siguen la recomendación de la 1a Conferencia Estratégica EFLM (Milán 2014) [17].
Los laboratorios participantes han mejorado su prestación a lo largo de los años, como indican el mayor grado de cumplimiento de las EPA (Figura 1) y las desviaciones decrecientes respecto al valor diana obtenidas. Probablemente el haber utilizado el criterio derivado de la VB para evaluar los resultados favoreció esta mejora.
A pesar de las críticas sobre la utilización de la VB como especificación de la prestación por ser demasiado estricta [17], en este trabajo se evidencia que son alcanzables por los laboratorios, para muchas magnitudes biológicas.
La disminución de la dispersión de métodos, el abandono de métodos obsoletos (enzimas) y el uso de la quimioluminiscencia en inmunoensayos (Figura 2) son factores que favorecen la mejora de las prestaciones.
La comparación de los programas EQA de la SEQCML con otros programas de distintas organizaciones es difícil porque los informes solo son accesibles a los participantes; por ello, en este estudio se presentan datos únicamente de programas que publican sus resultados en revistas internacionales o en páginas web de libre acceso. Otras dificultades radican en las diferencias en los materiales control distribuidos, en el criterio para formar grupos homogéneos, en los cálculos realizados y en las especificaciones de la calidad aplicadas para evaluar los resultados.
Así las DP% inferiores de SEQCML comparadas con ProBioQual (Tabla 2) probablemente se deban a que el programa español utiliza como especificación la VB, mientras que el programa francés utiliza la prestación actual de los métodos, que es más permisiva.
En cambio, las discrepancias observadas en los tres programas que usan controles conmutables con valores asignados por métodos de referencia certificados (Tabla 3) no se pueden explicar a la luz de los datos disponibles en este estudio.
Cuando las EPA están basadas en el estado del arte, se ha podido constatar que la mayoría de los programas no definen el “estado del arte” como la mejor prestación posible de los métodos usados por los participantes, tal como se recomendó en la 1a Conferencia estratégica EFLM de Milán [18], sino como la prestación actual de los métodos. Esta es una dificultad más para alcanzar la armonización.
Los datos mostrados en este estudio ponen de manifiesto que, a pesar de la que las prestaciones mejoren continuamente dentro de cada programa y se estén realizando esfuerzos para la armonización, los resultados obtenidos en diferentes programas para algunas magnitudes biológicas, todavía no están armonizados.
La armonización se conseguiría con el esfuerzo de todas las partes implicadas en la actividad del laboratorio médico: organizaciones internacionales que promueven normas y directrices, sociedades científicas que divulgan sus datos, la industria de diagnóstico in vitro que pone en el mercado métodos estandarizados y sistemas analíticos calibrados con patrones de trazabilidad documentada, y los laboratorios asistenciales que utilizan los mejores métodos con rigurosidad y protocolización.
Desde el año 1998 la comunidad internacional esta realizando esfuerzos para alcanzar la armonización, como queda plasmado en la siguiente documentación:
Directiva europea para la industria de diagnóstico in vitro (1998) que exige a los proveedores que aseguren la trazabilidad al nivel de referencia mas elevado, cuando sea posible
ISO 17511 (2003): In vitro diagnostic medical devices-Measurement of quantities biological samples – Metrological traceability of values assigned to calibration and control materials. Se publicó siguiendo los mismos requisitos de la directiva europea [19]
JCTLM (2002): creado por varias entidades internacionales que mantiene una base de datos de materiales de referencia, procedimientos analíticos y laboratorios de referencia de acuerdo con la norma ISO 17511 [20]
ICHCLR (2013): este consorcio tiene un portal global en el que se recoge la información actualizada sobre el estado de estandarización /armonización de las magnitudes biológicas y desarrolla protocolos para establecer la armonización de aquellas magnitudes biológicas para los que no existen materiales y métodos de referencia [21]
Nueva norma ISO/NP 21151 en desarrollo, en la que se defina los protocolos a seguir para asegurar la armonización de las magnitudes sin materiales ni métodos de referencia [19]
Los programas EQA juegan un importante papel en la vigilancia de la armonización de las prestaciones del laboratorio médico, pero se debería potenciar el uso de controles conmutables con valores de referencia certificados siempre que fuera posible y aplicar las especificaciones de la prestación analítica recomendadas.
Conclusiones
Los laboratorios participantes en los programas EQA de la SEQCML han mejorado notablemente su prestación a lo largo de los 30 años de experiencia.
Las especificaciones derivadas de la variación biológica son alcanzables por muchos laboratorios en nuestro país. Para las magnitudes biológicas sin datos de VB conocidos, se utiliza el estado del arte actual y no el mejor posible.
Los organizadores de programas EQA también deberían sumarse al esfuerzo de armonización, facilitando la información sobre sus resultados a otros profesionales interesados y facilitando la comparación entre las organizaciones.
-
Financiación de la investigación: No declarada.
-
Contribución de los autores: Todos los autores aceptan la responsabilidad sobre la totalidad de lo contenido en el manuscrito enviado, habiendo aprobado la totalidad de ellos su presentación.
-
Conflicto de intereses: Los autores declaran no tener ningún conflicto de intereses.
-
Aprobación Comité Ético: No procede en este estudio.
-
Nota del artículo: La versión traducida del artículo puede encontrarse aquí: https://doi.org/10.1515/almed-2020-0019
Referencias
1. Ramon F, Alsina MJ, Areal R, Cortés M, Navarro JM, Salas A. Evaluación del IV programa de control de calidad interlaboratorios de la SEQC. Quim Clin 1984;3:82–116.Suche in Google Scholar
2. Panthegini M, Sandberg S. Defining analytical performance specifications 15 years after Stockholm conference. Clin Chem Lab Med 2015;53:829–32. https://doi.org/10.1515/cclm-2015-0303.Suche in Google Scholar PubMed
3. Jones GRD, Albarede S, Kesseler D, MacKenzie F, Mammen J, Pedersen M, et al. Analytical performance specifications for external quality assessment- definitions and descriptions. Clin Chem Lab Med 2017;55:949–55. https://doi.org/10.1515/cclm-2017-0151.Suche in Google Scholar PubMed
4. Buttner J, Borth R, Boutwell JH, Broughton P, Bowyer RC. Recomendación aprobada (1982) sobre control de calidad en química clínica. IFCC. Quim Clin 1983;2:87–93.Suche in Google Scholar
5. Minchinela J, Ricós C, Perich C, Fernández-Calle P, Álvarez V, Doménech MV, et al. Biological variation database and quality specifications for imprecision, bias and total error (desirable and minimum). The 2014 update. http://www.westgard.com/biodatabase-2014-update.html. [Accedido en 16 Nov 2019].Suche in Google Scholar
6. Fraser CG, Hyltoft Petersen P, Libeer JC, Ricós C. Proposals for setting generally applicable quality goals solely based on biology. Ann Clin Biochem 1997;34:8–12.10.1177/000456329703400103Suche in Google Scholar PubMed
7. Miller GW, Jones GRD, Horowitz GL, Weykamp C. Proficiency testing/External quality assessment: current challenges and future directions. Clin Chem 2011;57:1670–80. https://doi.org/10.1373/clinchem.2011.168641.Suche in Google Scholar PubMed
8. Comité de Programas externos SEQCML. Descripción General del Funcionamiento de los Programas de Bioquímica. Publicación anual. http://www.contcal.org.Suche in Google Scholar
9. Jansen R, Cobaert CM, Weykamp C, Thelen M. The quest for equivalence of test results: the pilgrimage of the Dutch Calibration 2000 program for metrological traceability. Clin Chem Lab Med 2018;56:1673–84. https://doi.org/10.155/cclm-2017-0796.Suche in Google Scholar
10. Empower project: http://www.stt-consulting.com/news.php?rubriek=8.Suche in Google Scholar
11. Referenz institut für Bioanalytik (RfB): http://www.rfb.bio/cgi/surveys?searchType=rv_type&rv_type=KS&analyte=all&year=2018.Suche in Google Scholar
12. Matar G, Poggi B , Meley R, Bon C, Chardon L, Chikh Karim, et al. Uncertainty in measurement for 43 biochemistry, immunoassay, and hemostasis routine analytes evaluated by a method using only external quality assessment data. Clin Chem Lab Med 2015;53:1725–36. https://doi.org/10.1515/cclm-2014-0942.Suche in Google Scholar PubMed
13. Weykamp C, Secchiero S, Plebani M, Thelen M, Cobbaert C, Thomas A, et al. Analytical performance of 17 general chemistry analytes across countries and across manufacturers in the INPUtS project of EQA organizers in Italy, the Netherlands, Portugal, United Kingdom and Spain. Clin ChemLabMed 2017;55:203–11. https://doi.org/10.1515/cclm-2016-0220.Suche in Google Scholar PubMed
14. De Grande LAC, Goosens K, Van Uytfanghe K, Stöckl D, Thienpont LM. The Empower project: a new way of assessing and monitoring test comparability and stability. Clin Chem Lab Med 2015;53:1197–204. https://doi.org/10.1515/cclm-2014-0959.Suche in Google Scholar PubMed
15. Miller WG, Myers GL, Ashwood ER, Killeen AA, Wang E, Ehlers GW, et al. State of the art in trueness and interlaboratory harmonization for 10 analytes in general clinical chemistry. Arch Pathol Lab Med 2008;132:838–46.10.5858/2008-132-838-SOTAITSuche in Google Scholar PubMed
16. Van Houcke SK, Rustad P, Stepman HC, Kristensen G, Stöckl D, Rooras TH, et al. Calcium, magnesium, albumin and total protein measurement in serum as assessed with 20 fresh-frozen single-donation sera. Clin Chem 2012;58:1597–603. https://doi.org/10.1373/clinchem.2012.189670.Suche in Google Scholar PubMed
17. Carobene A. Reliability of biological variation data available in an online database: need to improvement. Clin Chem Lab Med 2015;53:871–7. https://doi.org/10.1515/cclm-2014-1133.Suche in Google Scholar PubMed
18. Sandberg S, Fraser CG, Horwath AR, Jansen R, Jones G, Oostehuiss W, et al. Defining analytical performance specifications–Consensus of the 1st Strategic conference EFLM. Clin Chem Lab Med 2015;53:833–5. https://doi.org/10.1515/cclm-2015-006.Suche in Google Scholar
19. International Organization for Standarization. www.iso.org.Suche in Google Scholar
20. Joint Committee for Traceability in Laboratory Medicine. https://www.bipm.org/en/committees/jc/jctlm/ [Accedido en 06 Nov 2019].Suche in Google Scholar
21. The International Consortium for Harmonization of Clinical Laboratory Results. www.harmonization.net.Suche in Google Scholar
Material Suplementario
La versión en línea de este artículo ofrece material suplementario (https://doi.org/10.1515/almed-2019-0024).
© 2020 Carmen Perich Alsina et al., published by De Gruyter, Berlin/Boston
This work is licensed under the Creative Commons Attribution 4.0 International License.
Artikel in diesem Heft
- Editorial
- The role of laboratory medicine specialists in the COVID-19 pandemic
- El profesional de la Medicina de Laboratorio ante la pandemia por COVID-19
- Laboratory medicine resilience during coronavirus disease 2019 (COVID-19) pandemic
- La capacidad de resiliencia de la medicina de laboratorio durante la pandemia de la enfermedad por coronavirus (COVID-19) iniciada en 2019
- Review / Artículo de Revisión
- Biomarkers of male hypogonadism in childhood and adolescence
- Biomarcadores de hipogonadismo masculino en la infancia y la adolescencia
- Original Article / Artículo Original
- Spanish society of laboratory medicine external quality assurance programmes: evolution of the analytical performance of clinical laboratories over 30 years and comparison with other programmes
- Programas de garantía externa de la calidad SEQCML. Evolución de las prestaciones analíticas de los laboratorios clínicos a lo largo de 30 años y comparación con otros programas
- Influence of study model, baseline catalytic concentrations and analytical system on the stability of serum alanine aminotransferase
- Estabilidad de la alanina aminotransferasa en suero. Efecto del modelo de estudio, la concentración catalítica inicial y la plataforma analítica
- Assessment of a change of protocol of prenatal screening by inclusion of non-invasive prenatal diagnosis
- Valoración de un cambio de protocolo del cribado prenatal mediante la inclusión del diagnóstico prenatal no invasivo
- Case Report / Caso Clínico
- Cystinuria: urine sediment as a diagnostic test
- Cistinuria: sedimento de orina como herramienta diagnóstica
- Letter to the Editor / Carta al Editor
- Unnecessary test ordering in clinical trials: human chorionic gonadotropin as an example
- Realización de pruebas innecesarias en los ensayos clínicos: hCG como ejemplo
Artikel in diesem Heft
- Editorial
- The role of laboratory medicine specialists in the COVID-19 pandemic
- El profesional de la Medicina de Laboratorio ante la pandemia por COVID-19
- Laboratory medicine resilience during coronavirus disease 2019 (COVID-19) pandemic
- La capacidad de resiliencia de la medicina de laboratorio durante la pandemia de la enfermedad por coronavirus (COVID-19) iniciada en 2019
- Review / Artículo de Revisión
- Biomarkers of male hypogonadism in childhood and adolescence
- Biomarcadores de hipogonadismo masculino en la infancia y la adolescencia
- Original Article / Artículo Original
- Spanish society of laboratory medicine external quality assurance programmes: evolution of the analytical performance of clinical laboratories over 30 years and comparison with other programmes
- Programas de garantía externa de la calidad SEQCML. Evolución de las prestaciones analíticas de los laboratorios clínicos a lo largo de 30 años y comparación con otros programas
- Influence of study model, baseline catalytic concentrations and analytical system on the stability of serum alanine aminotransferase
- Estabilidad de la alanina aminotransferasa en suero. Efecto del modelo de estudio, la concentración catalítica inicial y la plataforma analítica
- Assessment of a change of protocol of prenatal screening by inclusion of non-invasive prenatal diagnosis
- Valoración de un cambio de protocolo del cribado prenatal mediante la inclusión del diagnóstico prenatal no invasivo
- Case Report / Caso Clínico
- Cystinuria: urine sediment as a diagnostic test
- Cistinuria: sedimento de orina como herramienta diagnóstica
- Letter to the Editor / Carta al Editor
- Unnecessary test ordering in clinical trials: human chorionic gonadotropin as an example
- Realización de pruebas innecesarias en los ensayos clínicos: hCG como ejemplo

